
Autorzy publikacji.
Publikacja pt. "Human EXOG Possesses Strong AP Hydrolysis Activity: Implication on Mitochondrial DNA Base Excision Repair", autorstwa naukowców z Zakładu Biologii Strukturalnej Miedzyuczelnianego Wydziału Biotechnologii UG i GIMed: dra hab. Michała R. Szymańskiego, prof. UG i dr Anny Karłowicz, została opublikowana w prestiżowym czasopiśmie naukowym Journal of the American Chemical Society (JACS).
Link do publikacji: https://doi.org/10.1021/jacs.2c10558
Streszczenie
Mitochondria są niezbędne do życia komórki eukariotycznej ze względu na ich kluczową rolę w zasadniczych szlakach metabolicznych. Bliskość łańcucha oddechowego, który jest źródłem reaktywnych form tlenu (ROS) w mitochondriach, sprawia, że DNA mitochondrialny (mtDNA) jest znacznie bardziej narażony na stres oksydacyjny niż DNA jądrowy. Odkrycie, że nienaprawione uszkodzenia prowadzą do destabilizacji genomu mitochondrialnego, a w rezultacie do starzenia się i wielu poważnych chorób u ludzi, rozpoczęło intensywne badania nad mechanizmami naprawy mtDNA. Nadal jednak procesy naprawcze w mitochondriach nie zostały w pełni poznane i wiele fundamentalnych pytań nadal wymaga odpowiedzi.
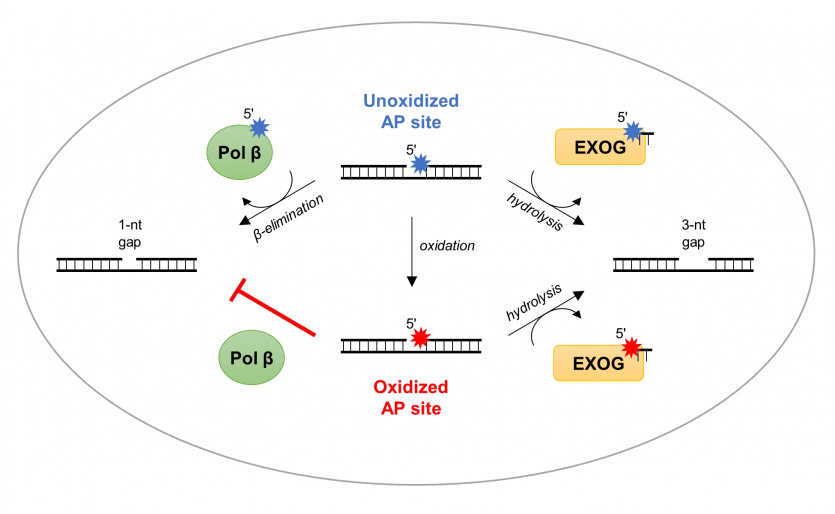
Większość uszkodzeń oksydacyjnych w mtDNA jest naprawiana dzięki ścieżce wycięcia zasady (ang. Base Excision Repair, BER), w którą zaangażowanych jest wiele enzymów. Jednak enzym mitochondrialny odpowiedzialny za usuwanie fosforanu deoksyrybozy (dRP) z końca 5’ nie został dotychczas opisany. 5’-dRP tworzy się po usunięciu uszkodzonej zasady (tworząc w ten sposób miejsce AP) oraz nacięciu szkieletu cukrowo-fosforanowego DNA.
- Dzięki analizom strukturalnym i enzymatycznym w naszej pracy pokazaliśmy, że ludzka mitochondrialna egzonukleaza EXOG ma bardzo silną aktywność usuwania dRP. W przeciwieństwie do kanonicznych liaz dRP (np. naprawcza polimeraza Pol β w jądrze komórkowym), które usuwają wyłącznie nienaruszone dRP, EXOG jest zdolne do wycięcia różnych miejsc AP: (1) dRP, (2) deoksyrybonolaktonu dL – utlenionej forma dRP, oraz (3) tetrahydrofuranu THF – syntetycznego analogu dRP. Rozwiązaliśmy strukturę krystaliczną EXOG w kompleksie z DNA zawierającego THF, jak i z częściową przerwą nukleotydową – tłumaczą autorzy publikacji. - Otrzymane dane strukturalne wraz z analizami biochemicznymi pozwoliły nam na zaproponowanie mechanizmu aktywności EXOG na substratach DNA zawierających różne uszkodzenia. Pokazaliśmy, że dzięki kontrolowanej 5’-egzonukleolitycznej aktywności EXOG nacina trzecie wiązanie fosfodiestrowe od miejsca AP, co pozwala na usunięcie uszkodzenia w mtDNA niezależnie od jego rodzaju – dodają.
Praca powstała w ramach grantu POLONEZ 2 Narodowego Centrum Nauki (NCN), którego dr hab. Michał R. Szymański, prof. UG był kierownikiem.
